贝拉西普(Belatacept)在国内上市了吗,贝拉西普(Belatacept)于2011年6月15日获得美国食品药品监督管理局(FDA)批准上市,目前国内未上市。
近年来,随着医学科技的不断进步,肾脏移植已成为治疗晚期肾病的有效手段之一。由于免疫系统的复杂性,移植后的器官排斥问题依然是困扰医学界的重要挑战之一。贝拉西普(Belatacept)作为一种新型的免疫抑制剂,在肾移植患者中预防器官排斥的效果备受关注。目前,有关贝拉西普在国内是否已经上市的问题,成为了学术界和患者关注的焦点之一。
1. 贝拉西普的作用机制及优势
贝拉西普是一种CTLA-4Ig类的免疫抑制剂,通过阻断T细胞的活化和增殖,从而抑制免疫系统对异体器官的排斥反应。相比传统的免疫抑制剂如环孢素和他克莫司,贝拉西普不会影响肾脏功能,且不增加患者罹患病毒感染的风险,因此被认为是一种更为安全和有效的选择。
2. 国内外临床研究进展
在国际上,贝拉西普已经被广泛应用于肾脏移植患者,并取得了显著的临床效果。多项研究显示,与传统免疫抑制剂相比,贝拉西普能够降低患者的长期肾移植排斥风险,同时减少药物相关的不良反应。尽管其在国际上的应用前景广阔,但在中国大陆地区,贝拉西普尚未正式上市,相关的临床应用和研究仍处于起步阶段。
3. 上市前景及挑战
尽管贝拉西普在国际上的临床数据表现出色,但要在中国市场上市,还需面临一些挑战。首先是药物的注册审批流程和临床试验要求,这需要与国内相关政策和规定相符合。其次是在临床实践中,如何有效推广和应用贝拉西普,以确保其在中国患者中的安全性和有效性。
总体而言,贝拉西普作为一种创新的肾移植免疫抑制剂,展现出了显著的优势和潜力。尽管目前在中国尚未正式上市,但随着国内医疗技术和政策的进步,相信未来贝拉西普有望为广大需要肾脏移植治疗的患者带来新的希望和选择。

 全部分类
全部分类

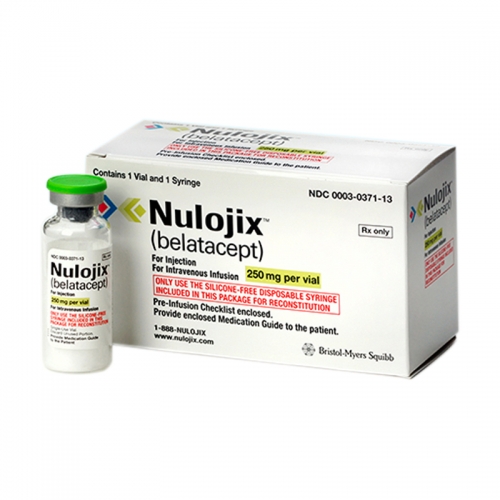
 美国施贵宝
美国施贵宝
 美国惠氏
美国惠氏
 瑞士诺华制药
瑞士诺华制药
 美国罗氏制药集团
美国罗氏制药集团


 粤ICP备2021070247号
粤ICP备2021070247号
