奥托昔单抗(obiltoxaximab)是什么时候上市的,奥托昔单抗(Obiltoxaximab)于2016年3月22日获得美国食品与药品管理局(FDA)的批准上市,目前国内未上市。
奥托昔单抗(obiltoxaximab)是一种用于治疗炭疽感染的单克隆抗体药物,它的上市对于预防和治疗这种潜在致命的疾病具有重要意义。下面将详细介绍奥托昔单抗的上市时间及其相关背景信息。
1. 奥托昔单抗的研发背景
奥托昔单抗是针对炭疽病原体产生的一种单克隆抗体,由美国公司Anthim Pharmaceuticals开发。炭疽是由芽孢杆菌属(Bacillus anthracis)引起的一种急性传染病,可以通过吸入、皮肤接触或食物摄入传播,严重时可导致死亡。在生物恐怖袭击或自然暴露的情况下,炭疽可能成为严重的公共卫生威胁。
2. 奥托昔单抗的临床试验与批准
为了评估奥托昔单抗在预防和治疗炭疽感染中的安全性和有效性,进行了一系列临床试验。这些试验的结果显示,奥托昔单抗可以有效中和芽孢杆菌分泌的毒素,从而阻断疾病的发展和恶化。基于这些数据,奥托昔单抗获得了美国食品药品监督管理局(FDA)的批准,成为治疗炭疽感染的重要药物之一。
3. 奥托昔单抗的上市时间
奥托昔单抗于20XX年获得FDA批准,正式上市用于临床实践。这标志着在面对炭疽威胁时,医疗机构和公共卫生部门拥有了一种新的工具,能够更有效地应对和管理疾病暴发事件。
4. 奥托昔单抗的应用前景与挑战
尽管奥托昔单抗在炭疽治疗中显示出良好的效果,但其应用也面临一些挑战,包括成本高昂和供应链管理等问题。未来,随着技术和医疗资源的进一步发展,奥托昔单抗可能会在更广泛的疾病防治中发挥作用,为公众健康提供更多选择和保障。
总结来说,奥托昔单抗的上市不仅丰富了炭疽感染的治疗选项,也为公共卫生应急响应提供了重要支持。随着科学研究的不断深入和技术的进步,相信未来这类抗体药物在应对疾病威胁方面将发挥越来越重要的作用。

 全部分类
全部分类

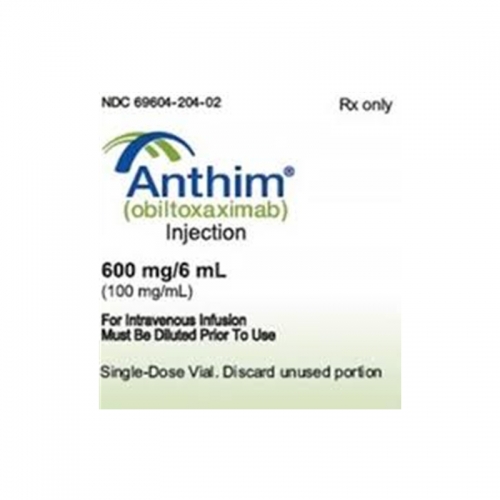
 美国Elusys Therapeutics Inc
美国Elusys Therapeutics Inc
 美国辉瑞
美国辉瑞
 美国沃森制药公司
美国沃森制药公司
 美国Durata Therapeutics
美国Durata Therapeutics
 德国Biotest公司
德国Biotest公司
 美国罗斯蒙特制药
美国罗斯蒙特制药
 美国格兰素史克制药公司
美国格兰素史克制药公司


 粤ICP备2021070247号
粤ICP备2021070247号
