羧甲麦芽糖(ferric carboxymaltose)Injectafer国内上市时间,羧甲麦芽糖(ferric carboxymaltose)于2007年6月首先在德国上市,于2013年7月获FDA批准在美国上市,于2022年11月24日国内获批上市。
羧甲麦芽糖(ferric carboxymaltose)Injectafer是一种用于治疗缺铁性贫血的药物。它在国外已经广泛应用并取得了良好的疗效,而在国内的上市时间备受关注。本文将对羧甲麦芽糖(ferric carboxymaltose)Injectafer的国内上市时间进行简要介绍和探讨。
1. 国内上市时间尚未确定
羧甲麦芽糖(ferric carboxymaltose)Injectafer作为一种新型的缺铁性贫血治疗药物,备受国内医疗界和患者关注。目前尚未确定它在国内的上市时间。尽管在国外的一些市场已经上市并应用广泛,但每个国家的药物审批和上市程序都各不相同。
2. 国内上市时间取决于药物审批流程
羧甲麦芽糖(ferric carboxymaltose)Injectafer的国内上市时间主要取决于国内的药物审批流程。在中国,药物上市需要经过一系列的审批和评价程序,包括临床试验、药物注册、药物审评等。此外,还需要考虑相关政策法规和其他监管要求。这些程序的时间周期是相对较长的,因此需要一定的耐心等待。
3. 临床疗效和安全性证据的重要性
羧甲麦芽糖(ferric carboxymaltose)Injectafer作为一种新型药物,在国内上市前需要充分的临床疗效和安全性证据支持。这意味着需要进行大规模的临床试验,以评估其疗效和安全性。这些试验需要经过严格的设计和执行,并在不同地区的患者群体中进行验证。这些临床证据对于羧甲麦芽糖(ferric carboxymaltose)Injectafer国内上市的时间也起到至关重要的作用。
4. 期待羧甲麦芽糖(ferric carboxymaltose)Injectafer的国内上市
羧甲麦芽糖(ferric carboxymaltose)Injectafer作为一种治疗缺铁性贫血的药物,对于国内很多患者来说具有重要意义。它能够有效补充体内的铁元素,改善患者的贫血状况。在国外的临床应用中,羧甲麦芽糖(ferric carboxymaltose)Injectafer已经得到了广泛认可,并展现出良好的疗效和安全性。因此,我们对其国内上市充满期待,并希望能够尽快为国内的患者提供这一新的治疗选择。
总结起来,羧甲麦芽糖(ferric carboxymaltose)Injectafer作为一种用于治疗缺铁性贫血的新型药物,其国内上市时间目前尚未确定。国内上市的时间将受药物审批流程、临床疗效和安全性证据等多个因素的影响。尽管如此,我们对羧甲麦芽糖(ferric carboxymaltose)Injectafer的国内上市充满期待,并期望能够尽快为需要治疗的患者提供这一创新的治疗选择。
 羧甲麦芽糖的相关介绍
羧甲麦芽糖的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2024-02-15 09:58:59 更新
 全部分类
全部分类



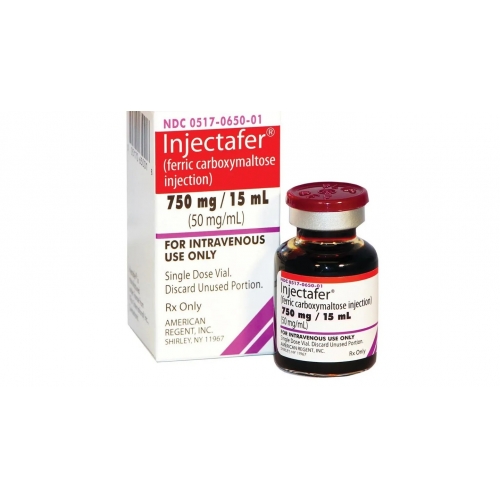
 美国REGENT
美国REGENT
 德国MEDICE
德国MEDICE
 老挝卢修斯制药
老挝卢修斯制药

 美国阿吉奥斯制药公司
美国阿吉奥斯制药公司
 法国赛诺菲
法国赛诺菲

 粤ICP备2021070247号
粤ICP备2021070247号
