Asciminib(阿西米尼)国内有没有上市,Asciminib(Asciminib)于2021年10月底获批在美国上市,全球首个获批的STAMP抑制剂,目前为止,阿西米尼还没有在国内上市。
近年来,白血病治疗领域不断迎来创新药物。其中,Asciminib(阿西米尼)作为一种新型的治疗慢性髓样白血病(CML)的药物备受关注。此药物是否已在国内上市成为广大患者和医护人员关注的焦点。下文将就Asciminib(阿西米尼)在国内的上市情况作详细介绍。
1. Asciminib(阿西米尼):一款治疗白血病的创新药物
Asciminib(阿西米尼)属于一类名为BCR-ABL酪氨酸激酶抑制剂的药物,被广泛应用于治疗慢性髓样白血病患者。相较于传统的CML治疗药物,Asciminib(阿西米尼)具有更为精准的靶向治疗作用,且在耐药性和特定病例治疗上具备独特优势,为CML患者带来了新的希望。
2. 国内临床研究情况
针对Asciminib(阿西米尼)在国内的上市情况,一些临床研究已经在中国展开。通过包括中国在内的临床试验,Asciminib(阿西米尼)在临床疗效及安全性上都取得了积极的结果,为其在国内的上市奠定了良好的基础。
3. 上市进展及临床应用
截至目前,Asciminib(阿西米尼)尚未在中国正式获得上市许可。该药的临床试验结果显示出很大的潜力,许多患者和医生对其临床应用寄予厚望。未来,随着临床研究的不断深入以及相关审批流程的推进,Asciminib(阿西米尼)有望在中国获得上市许可,为更多的患者带来希望。
4. 后续展望与建议
对于Asciminib(阿西米尼)在中国上市的后续发展,需要加强研究与临床实践的结合,以进一步验证其在中国患者群体中的疗效和安全性。同时,相关药品监管部门也应加速审批进程,将Asciminib(阿西米尼)早日引入中国市场,让更多的CML患者从中受益。
结语
白血病治疗领域的不断创新为患者带来了新的曙光,Asciminib(阿西米尼)作为新型的治疗药物有望在未来成为CML患者的重要治疗选择。随着国内临床研究和审批程序的不断推进,相信Asciminib(阿西米尼)的上市将为患者带来更多治疗机会和希望。
 阿西米尼的相关介绍
阿西米尼的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2024-02-04 08:39:46 更新
 全部分类
全部分类



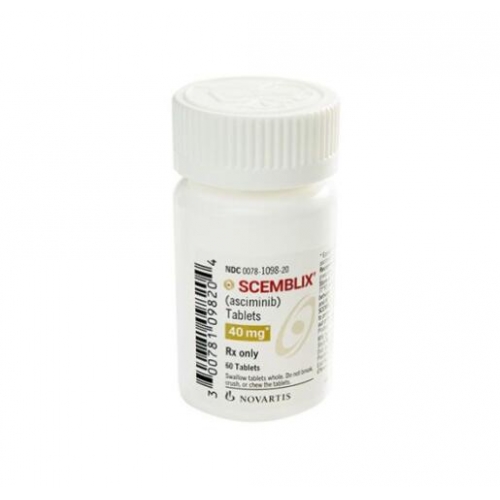
 瑞士诺华制药
瑞士诺华制药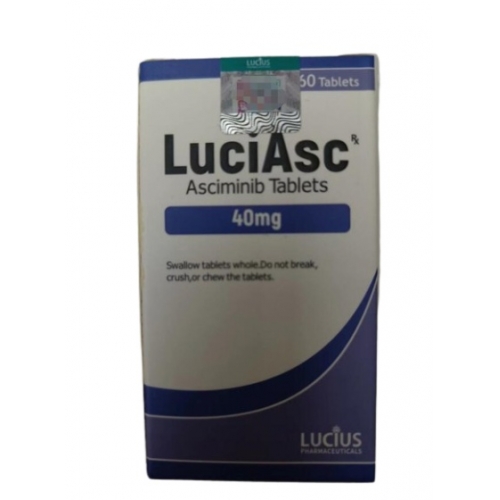
 老挝卢修斯制药
老挝卢修斯制药
 日本武田
日本武田
 美国吉利德
美国吉利德
 印度natco
印度natco
 美国施贵宝
美国施贵宝
 美国迈兰
美国迈兰


 粤ICP备2021070247号
粤ICP备2021070247号
