达妥昔单抗(Dinutuximab)国内上市时间,达妥昔单抗(Dinutuximab)于2015年3月获得了美国FDA的加速批准,国内上市时间是2021年8月12日。
达妥昔单抗(Dinutuximab)是一种针对高危神经母细胞瘤的抗体药物,其成为了一线治疗方案的关键之一。该药物的国内上市时间备受关注,下面将对达妥昔单抗在国内上市的时间进行简要介绍和探讨。
1. 达妥昔单抗(Dinutuximab)的研发背景和意义
2. 国内临床试验和安全性评估
3. 国内上市时间预测与问题
4. 对病患和医学界的希望
首先,让我们来了解一下达妥昔单抗(Dinutuximab)的研发背景和意义。神经母细胞瘤是一种罕见但危险的儿童肿瘤,其治疗一直是医学界的难题之一。而达妥昔单抗作为一种抗体药物,能够结合并清除肿瘤细胞,有效阻止病情的进展。临床试验显示,达妥昔单抗与传统治疗相比,在提高患儿的生存率和减少病情复发方面取得了显著的突破。
国内也积极开展了对达妥昔单抗的临床试验和安全性评估,以确保该药物在中国患者中的有效性和安全性。这些临床试验结果对该药物的国内上市时间具有重要作用。在临床试验阶段,医学界和患者对达妥昔单抗的表现和优势深感期待。
国内上市时间预测和问题也备受关注。由于国内药物监管体系和审批流程的特殊性,药物上市时间的推进可能面临一些挑战和延迟。此外,价格和供应等因素也可能会影响患者对达妥昔单抗的获得和使用。
不过,尽管存在种种难题,对病患和医学界来说,达妥昔单抗的国内上市仍然是一个重要的里程碑。这将为高危神经母细胞瘤的患者提供一种新的治疗选择,为抗击这一疾病带来新的希望。同时,通过引入国内上市的达妥昔单抗,也有望进一步推动国内儿童肿瘤治疗的研究和发展。
总而言之,达妥昔单抗(Dinutuximab)国内上市时间备受期待,其将为高危神经母细胞瘤患者带来新的治疗选择和希望。尽管面临一些挑战和延迟,但我们对国内临床试验的进展和相关药物监管的推进保持乐观。相信在不久的将来,达妥昔单抗将能够在中国上市,并为患者带来福音。
 达妥昔单抗的相关介绍
达妥昔单抗的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2024-01-06 13:50:48 更新
 全部分类
全部分类



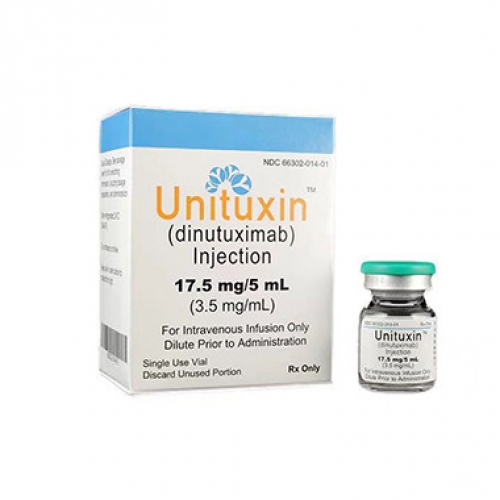
 瑞士罗氏
瑞士罗氏
 德国Rentschler Biotechnologie GmbH
德国Rentschler Biotechnologie GmbH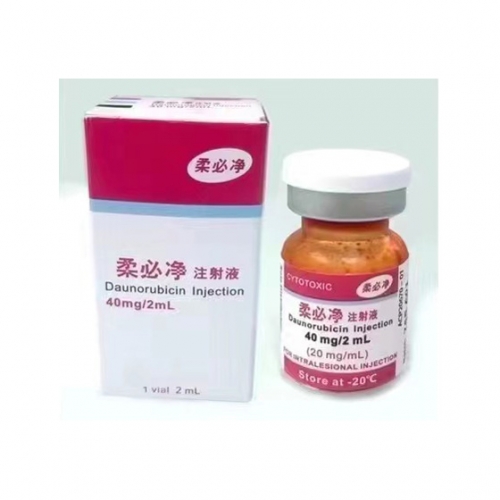
 美国纳米
美国纳米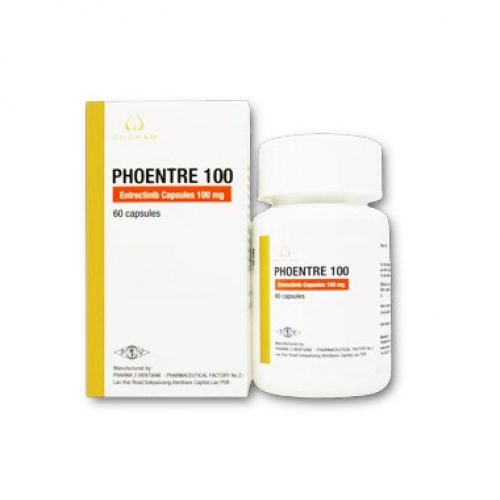
 老挝第二制药
老挝第二制药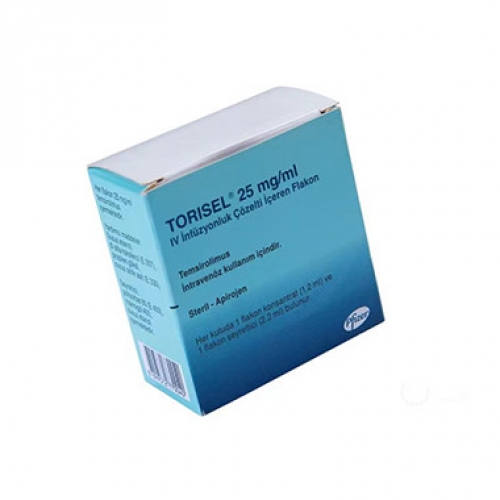
 美国辉瑞
美国辉瑞
 日本化药
日本化药

 粤ICP备2021070247号
粤ICP备2021070247号
