贝达喹啉最早于2012年获得美国食品和药物管理局(FDA)的紧急使用批准,用于治疗MDR-TB患者。此后,一系列临床试验与研究证实了贝达喹啉的疗效和安全性,使其得以在全球范围内上市和使用。
在贝达喹啉上市之前,结核病的一线治疗药物包括异烟肼、利福平和吡嗪酰胺等。然而,许多耐药结核病株对这些药物产生了耐药性。贝达喹啉的机制是通过干扰细菌的能量代谢来杀死结核杆菌,从而克服了耐药性的问题。它可以与传统药物一同使用,提供一种更有效的治疗选择。
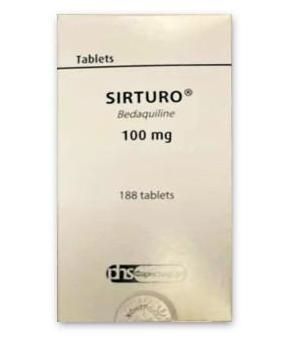
贝达喹啉在国际上的上市时间略有不同。在欧盟,该药物于2014年获准面向欧洲市场。在美国,FDA于2012年首次批准该药物。目前,贝达喹啉已经在超过30个国家获得批准,并进入市场。
然而,正如任何新药物一样,贝达喹啉也存在着一些潜在的副作用和风险。常见的不良反应包括恶心、呕吐、心律失常、视力问题和肝脏损伤等。因此,在使用贝达喹啉时,需要密切监测患者的身体反应,并确保医生的指导和监督下使用。
此外,贝达喹啉的使用还受到一些限制。根据世界卫生组织的建议,其主要推荐用于肺结核患者中的成年人,特别是耐多药结核病或出现药物不耐受的情况。对于儿童、孕妇、哺乳期妇女、以及有心律失常或视力问题的患者,则需格外谨慎使用。
总之,贝达喹啉的上市填补了目前结核病治疗领域的一项重大需求。它是一种有希望改变MDR-TB治疗方式的新型药物。它的独特机制和全球范围内的临床试验支持了它作为耐药结核病的有力治疗药物。然而,在使用过程中需要注意副作用和限制,确保患者的安全。随着新的研究和进一步的临床验证,预计贝达喹啉将为MDR-TB患者提供更好的治疗选择。
 贝达喹啉的相关介绍
贝达喹啉的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2023-10-25 16:43:50 更新
 全部分类
全部分类




 美国强生
美国强生

 美国麦迪西斯
美国麦迪西斯
 日本大冢
日本大冢
 美国迈兰
美国迈兰
 美国雅培
美国雅培
 印度Macleods
印度Macleods

 粤ICP备2021070247号
粤ICP备2021070247号
