替沃扎尼是一种口服的血管内皮生长因子受体(VEGFR)抑制剂。它通过抑制肿瘤上血液供应所需的新血管的生长来对抗癌细胞的增殖。替沃扎尼首次在Phase III临床试验中显示出了对晚期肾癌治疗的潜力,且相对于当前市场上的其他治疗方法,其不良反应更轻微,使得患者更易于接受。
然而,替沃扎尼的上市历程并不顺利。在2013年,替沃扎尼申请上市遭到了美国食品药品监管局(FDA)的拒绝。FDA在其拒绝函中提到,申请的临床数据不足以证明替沃扎尼的疗效优于当前市场上的其他药物,且存在一些潜在的安全风险。这个决定让替沃扎尼的上市前景变得不明朗。
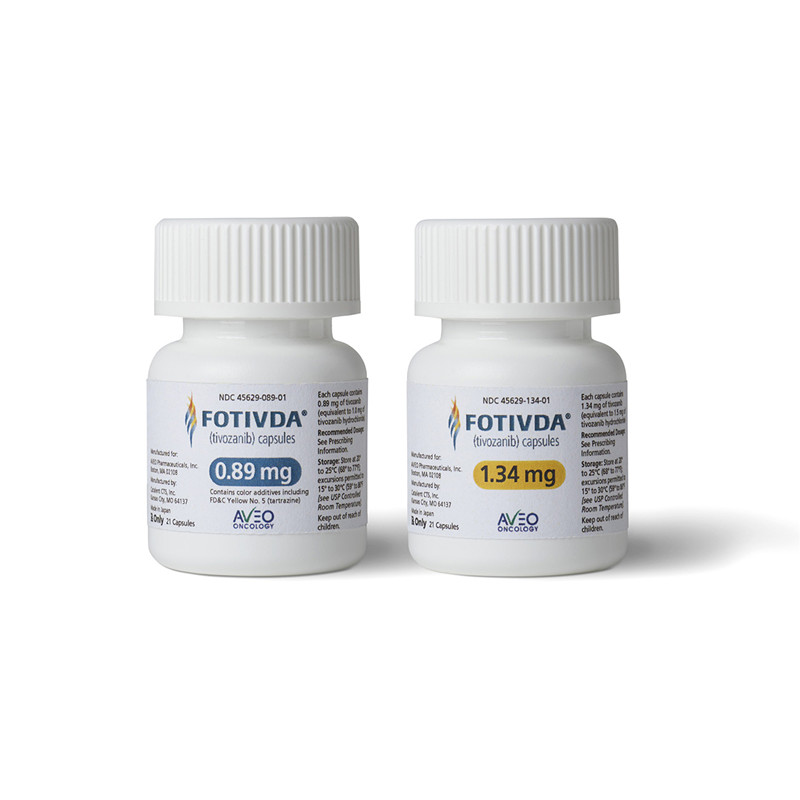
不过,替沃扎尼的制药公司AVEO Oncology并没有放弃。在接到FDA拒绝函后,他们进行了进一步的研究,并提交了其他的临床数据以证明替沃扎尼的疗效和安全性。在2017年,替沃扎尼终于在欧洲得到了批准,并在欧洲多个国家上市销售。这是一个替沃扎尼的重要里程碑,也为其在其他市场的上市奠定了基础。
除了欧洲市场,替沃扎尼还在全球范围内进行了多项临床试验,包括在中国、南美和澳大利亚等地的Phase III试验。根据AVEO Oncology的消息,替沃扎尼在这些地区的试验结果也是积极的,且与欧洲市场的数据相吻合。
随着替沃扎尼在全球范围内的研究和临床试验的进展,许多人对其是否会在未来的某个时候获得美国FDA的批准并上市充满了期待。虽然之前遭到了拒绝,但是替沃扎尼的疗效和安全性数据的改进,有望为其重新申请上市提供了有利的条件。
总的来说,替沃扎尼是一种具有潜在市场潜力的肾癌治疗药物。虽然其在美国市场上市的进程遇到了一些困难,但在其他地区的上市成功和全球范围内的积极临床试验结果,给人们带来了一丝曙光。无论最终结果如何,替沃扎尼的研究和发展都将为肾癌患者提供更多治疗选择,并为肾癌的治疗领域带来新的希望。
 替沃扎尼的相关介绍
替沃扎尼的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2023-07-17 11:13:17 更新
 全部分类
全部分类



 美国AVEO
美国AVEO
 孟加拉珠峰制药
孟加拉珠峰制药
 老挝卢修斯制药
老挝卢修斯制药


 老挝第二制药
老挝第二制药
 美国辉瑞
美国辉瑞
 孟加拉碧康制药
孟加拉碧康制药
 孟加拉耀品国际
孟加拉耀品国际
 瑞士诺华制药
瑞士诺华制药

 粤ICP备2021070247号
粤ICP备2021070247号
