SER-109(fecal microbiota spores, live-brpk)国内上市时间,SER-109(Fecal Microbiota Spores, live-brpk)于2023年4月27日获得美国食品药品监督管理局(FDA)的批准上市,目前国内未上市。
SER-109是一种新型的治疗方法,专门用于处理艰难梭菌感染,该药物在国外已经显示出显著的疗效。在中国,人们也对其上市时间及其在治疗艰难梭菌感染中的应用充满期待。
SER-109在中国上市时间的消息引起了医学界和患者的广泛关注。这种新型治疗方法被认为可能带来全新的治疗选择,特别是对于那些反复发作或难以治愈的艰难梭菌感染患者而言,这意味着一线希望的到来。
1. SER-109的独特性及其机制
SER-109是一种利用人体肠道微生物组芽孢的生物制剂,其独特的机制被认为能够有效地调节肠道微生态,从而抑制艰难梭菌的再发和生长。这种疗法相较于传统抗生素具有显著的优势,因为它不会导致广谱抗生素引起的肠道微生态紊乱。
2. SER-109在国际上的临床研究成果
在国际上,SER-109已经进行了多项临床研究,结果显示在治疗难治性艰难梭菌感染方面具有显著的疗效。患者在接受完整疗程后,艰难梭菌感染的复发率显著降低,且疗效长期稳定。
3. 中国上市时间的预期
尽管在国际上已经有了积极的临床数据支持,但SER-109在中国的上市时间目前尚未确定。相关的注册和审批程序可能需要时间,医药企业和研究机构正在努力推进相关工作,以尽快将这一新治疗引入中国市场,造福更多的患者。
4. SER-109在艰难梭菌感染治疗中的意义
对于艰难梭菌感染患者而言,SER-109的上市将意味着一种新的治疗选择。相较于传统治疗方法,SER-109不仅可以显著降低复发率,还有望改善患者的生活质量。它可能成为治疗这类难治性感染的重要工具,为医生和患者带来新的希望。
在中国,对SER-109上市时间的期待和研究成果的关注正在逐步增加。随着相关研究的不断深入和注册进程的推进,相信这一创新治疗方法将尽快为中国的患者带来福音,为治疗艰难梭菌感染开辟新的前景。
 SER-109的相关介绍
SER-109的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2025-05-16 16:40:24 更新
 全部分类
全部分类



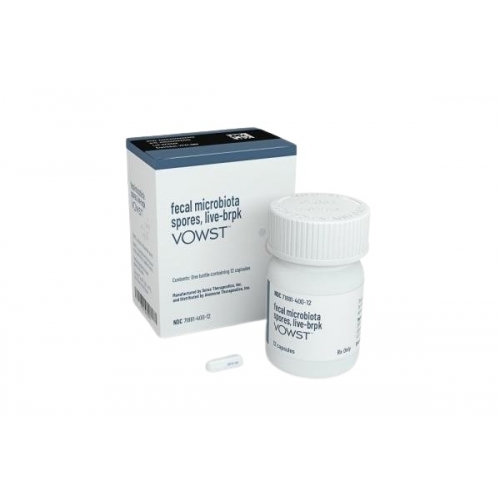
 美国Seres Therapeutics
美国Seres Therapeutics
 加拿大威朗制药
加拿大威朗制药
 德国Intendis
德国Intendis
 日本Astellas制药
日本Astellas制药
 瑞士Basilea
瑞士Basilea
 美国辉瑞
美国辉瑞
 德国默沙东
德国默沙东

 粤ICP备2021070247号
粤ICP备2021070247号
