Amvuttra(Vutrisiran)是什么时候上市的,Amvuttra(Vutrisiran)在2022年6月13日获得了美国食品和药物管理局(FDA)的批准上市,目前国内未上市。
Amvuttra(Vutrisiran)是一种治疗多发性神经病的新药物,对于患有家族性淀粉样变性(hATTR)的患者具有重要的治疗意义。它通过RNA干扰技术作用于TTR基因,从而减少异常TTR蛋白的产生,进而延缓疾病的进展。Amvuttra的上市对于这些患者来说,是一种新的希望和治疗选择。
1. Amvuttra(Vutrisiran)的研发历程
Amvuttra(Vutrisiran)的研发始于对家族性淀粉样变性(hATTR)的深入理解和治疗需求。该药物经过多年的临床试验和研究,证明其在降低TTR蛋白异常聚集方面的有效性和安全性。其研发历程经历了严格的审批流程和各项临床试验,以确保其在市场上的安全性和有效性。
2. Amvuttra(Vutrisiran)的上市批准
Amvuttra(Vutrisiran)获得了多国药品监管机构的批准,包括美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)。这些批准标志着这一药物已经完成了临床试验阶段,并证明了其在治疗hATTR患者中的显著疗效和安全性。药品上市意味着患者可以通过合法渠道获得这一创新的治疗选择。
3. Amvuttra(Vutrisiran)的市场推广与应用
Amvuttra(Vutrisiran)的上市为患有hATTR的患者带来了新的治疗希望。作为一种靶向TTR基因的RNA干扰药物,它不仅仅可以帮助延缓疾病的进展,还可以显著改善患者的生活质量。市场推广将进一步提升医疗专业人员对于hATTR治疗的认识,帮助更多患者及早接受有效的治疗。
Amvuttra(Vutrisiran)的上市标志着医学领域不断迈向创新和进步的里程碑。对于患有hATTR的患者及其家庭来说,这不仅是一种新的治疗选择,更是希望的象征。随着更多关于Amvuttra的临床应用和长期效果的研究逐步展开,相信它将为全球范围内的患者群体带来更多积极的变化和福音。
 Amvuttra的相关介绍
Amvuttra的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2024-09-03 14:23:54 更新
 全部分类
全部分类



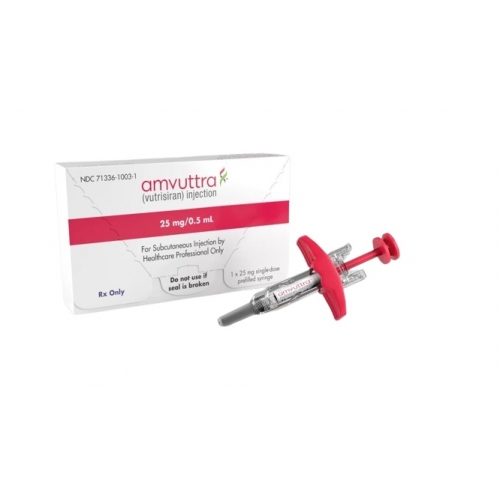
 美国艾拉伦公司
美国艾拉伦公司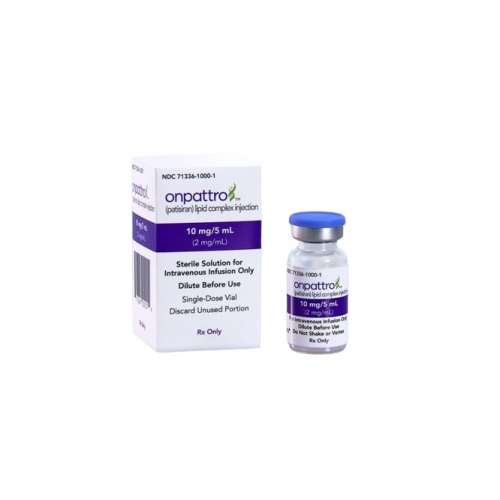
 美国Alnylam公司
美国Alnylam公司

 粤ICP备2021070247号
粤ICP备2021070247号
