依特立生(Eteplirsen)Exondys51的使用说明,依特立生(Eteplirsen)推荐剂量为30mg/kg,通过串联0.2微米过滤器,在35-60min内静脉输注给药,每周一次。
依特立生(Eteplirsen),商品名Exondys 51,是一种由美国食品和药物管理局(FDA)批准的新药,广泛应用于杜氏肌营养不良症(Duchenne muscular dystrophy,简称DMD)患者的治疗中。以下是关于依特立生(Eteplirsen)Exondys 51使用说明的详细介绍。
DMD是一种罕见而严重的遗传性疾病,主要影响男性。这种疾病导致身体逐渐丧失肌肉功能,最终导致无法行走和进行日常活动,甚至危及生命。长期以来,科学家们一直在寻找能够改善DMD患者病情的药物,而依特立生(Eteplirsen)Exondys 51就是首个获得FDA批准的新药。
1. 依特立生(Eteplirsen)Exondys 51的作用机制:
依特立生(Eteplirsen)Exondys 51是一种小分子核酸药物,通过改变个体基因表达,有助于修复和恢复患者体内缺失的dystrophin蛋白质。dystrophin蛋白质的缺失是DMD患者疾病进展的主要原因之一,而依特立生(Eteplirsen)Exondys 51可以在一定程度上纠正这种缺陷。
2. 使用方法和剂量:
依特立生(Eteplirsen)Exondys 51主要通过静脉注射给予患者。在开始使用前,必须确保患者的身体状态适合接受该药物的治疗。剂量的确定应由专业医生根据患者个体情况进行,一般情况下,每周一次的治疗会持续进行一段时间。
3. 注意事项和潜在的不良反应:
使用依特立生(Eteplirsen)Exondys 51时,患者和医生需要密切合作,并遵循医生的嘱咐。同时,应定期进行身体检查和监测,以确保药物的有效性和安全性。
尽管依特立生(Eteplirsen)Exondys 51经过了临床试验和FDA批准,但其使用过程中仍有可能出现一些不良反应。具体的不良反应类型和程度因人而异,常见的包括注射部位疼痛、感染、呕吐等。如果患者在治疗过程中出现任何不适或疑问,应及时与医生联系并告知情况。
4.
依特立生(Eteplirsen)Exondys 51的批准是对DMD患者及其家人的一大突破。作为首个获得FDA批准的新药,它为DMD患者提供了一种希望,可以延缓疾病的进展并提高他们的生活质量。对于使用该药物的患者来说,合理使用,并密切遵循医生的指导是至关重要的。通过积极的治疗和细心的监护,我们有理由相信依特立生(Eteplirsen)Exondys 51将为DMD患者带来更大的福祉。
 依特立生的相关介绍
依特立生的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2024-01-21 10:46:23 更新
 全部分类
全部分类



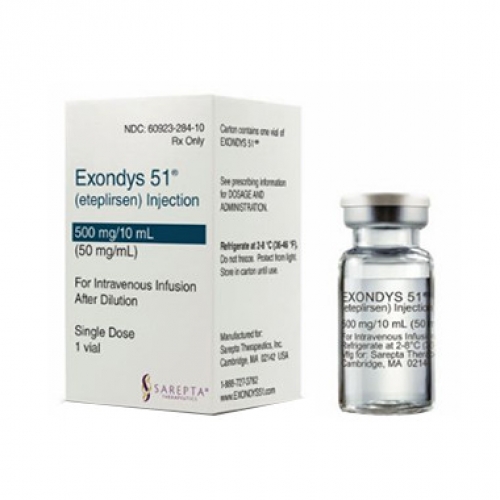
 美国sarepta
美国sarepta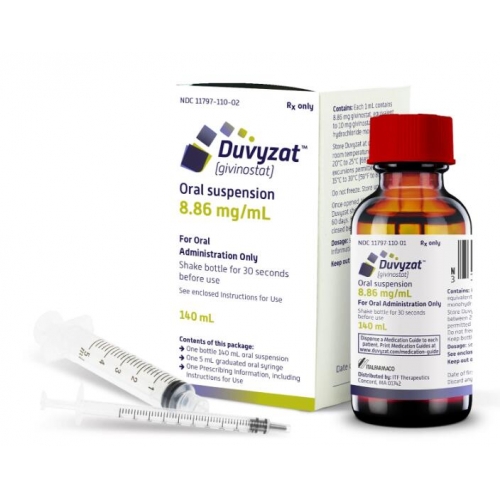
 意大利Italfarmaco制药集团
意大利Italfarmaco制药集团
 美国PTC Therapeutics
美国PTC Therapeutics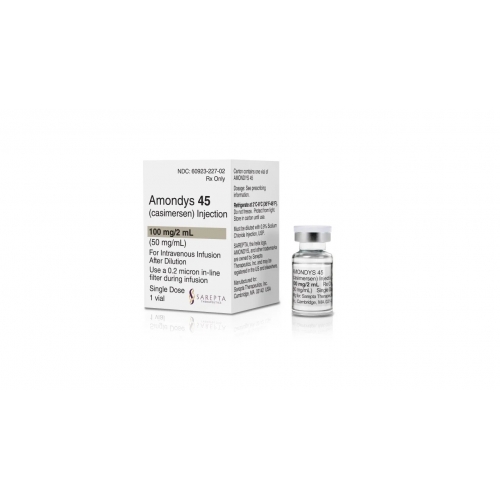
 美国Sarepta Therapeutics
美国Sarepta Therapeutics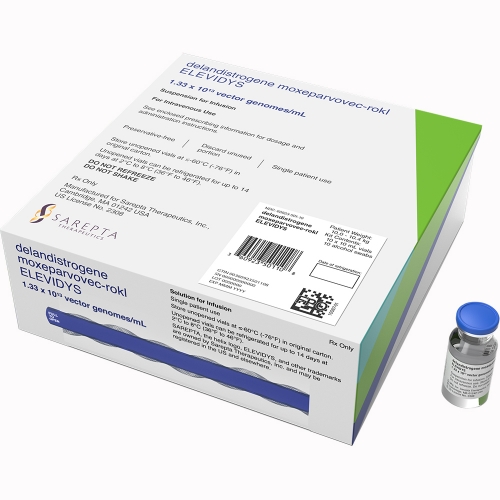

 印度Macleods
印度Macleods

 粤ICP备2021070247号
粤ICP备2021070247号
