速福达(Baloxavir marboxil)玛巴洛沙韦国内有没有上市,速福达(Baloxavir marboxil)由日本盐野义制药公司和罗氏联合研发,于2018年2月在日本获批上市,同年10月获美国批准上市。2021年4月,该药正式获得中国国家药品监督管理局批准,在中国市场上市(商品名为速福达)。
1. 快速发展的抗流感药物市场
近年来,随着甲型和乙型流感的流行,对于治疗流感的需求也日益增长。传统的抗流感药物如奥司他韦(Oseltamivir)和扎那米韦(Zanamivir)在一定程度上能够缓解症状,但也面临一些限制和不足。因此,科学家不断努力寻找更有效和安全的抗流感药物。
2. 特点与优势
速福达玛巴洛沙韦作为一种新型的抗流感药物,具有一些独特的特点和优势。它通过抑制流感病毒的复制,能够更快地减轻症状,并且能够在短时间内降低病毒载量。由于其独特的作用机制,速福达玛巴洛沙韦还具有较低的耐药性发展风险。
3. 国内上市情况
截至文章创作时,关于速福达玛巴洛沙韦在国内的上市情况尚未有具体的报告。这并不代表这种药物不会在将来进入中国市场。中国是世界上人口最多的国家之一,流感高发季节对于人们的健康和经济都会造成一定的影响。因此,速福达玛巴洛沙韦的上市有望在未来得到政府和药监机构的支持,并提供给需要的患者。
4. 研发与评估情况
速福达玛巴洛沙韦自问世以来,已经在一些国家得到了批准并上市。每个国家的药物上市程序和标准不尽相同,因此对于速福达玛巴洛沙韦在不同国家的上市情况需要具体考虑。在中国,药物的研发和上市通常需要经过严格的临床试验和审批程序,以确保药物的安全性和有效性。
速福达玛巴洛沙韦作为一种新型的抗流感药物,具有很大的潜力来改善甲型和乙型流感的治疗效果。虽然在本文创作时尚未获得关于速福达玛巴洛沙韦在国内的上市情况的明确信息,但考虑到中国庞大的人口和流感带来的影响,将来有望看到这种药物在中国市场上市。随着进一步的研发和评估,速福达玛巴洛沙韦有望为流感患者提供更好的治疗选择。
 玛巴洛沙韦的相关介绍
玛巴洛沙韦的相关介绍
注:本站所有内容仅供参考,不代表药直供立场(如有错漏,请帮忙指正),转载请注明出处。不作为诊断及治疗依据,不可替代专业医师诊断、不可替代医师处方。本站不承担由此导致的相关责任!
2024-01-06 11:39:06 更新
 全部分类
全部分类



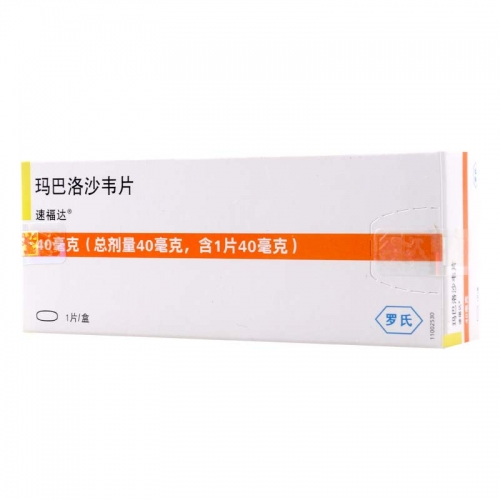
 瑞士罗氏
瑞士罗氏
 日本富士制药
日本富士制药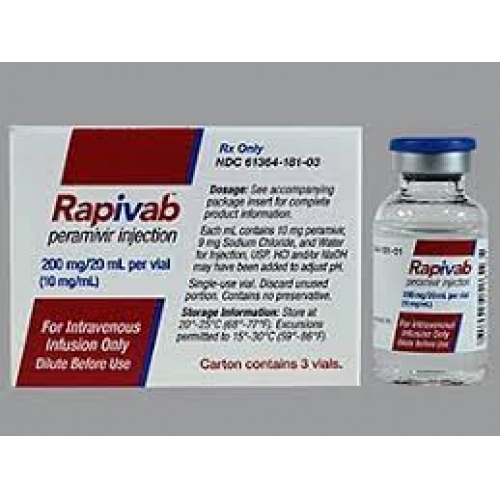
 美国BioCryst制药
美国BioCryst制药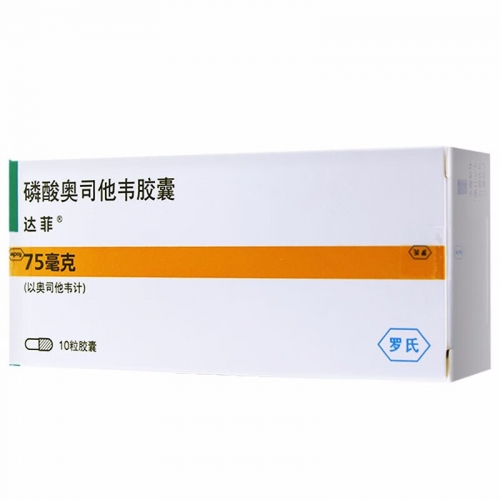


 粤ICP备2021070247号
粤ICP备2021070247号
