截至目前,索托拉西布尚未在中国国内上市。然而,该药物已经在美国获得了紧急使用授权(EUA),为那些在其他治疗方案失败后,并携带有KRAS G12C突变的晚期非小细胞肺癌(NSCLC)患者提供了一个新的治疗选择。
索托拉西布的研究始于早在2017年,当时的一项临床试验证实了这种靶向药物对KRAS变异的肺癌患者具有显著的治疗效果。随后,在2020年的一项重要的临床试验中,索托拉西布在参与的患者中显著延长了总生存期,数百名患者纳入试验后,取得了显著的疗效。
虽然索托拉西布在美国已经获得了紧急使用授权,但在中国国内的上市尚未获得批准。这可能是因为国内药品监管机构对药物的审批速度较慢,需要更多的数据来支持该药物的安全性和有效性。
尽管如此,索托拉西布的上市在中国国内仍具有巨大的潜力。中国是全球肺癌患者最多的国家之一,KRAS变异型肺癌在中国的患病率也相对较高。因此,索托拉西布的上市将为中国的肺癌患者提供一种新的治疗选择,有望改善他们的生活质量和生存率。
对于国内的肺癌患者来说,索托拉西布的上市意味着他们将有机会获得更加个体化和精准的治疗。靶向药物的优势在于减少了对患者的非特异性毒副作用,同时提高了治疗的有效性。相比传统的化疗,这对于那些长期饱受肺癌困扰的患者来说是一个巨大的突破。
然而,索托拉西布的上市也面临一些挑战。首先,该药物的价格可能较高,超出许多患者的负担能力。其次,肺癌治疗领域竞争激烈,其他类似的靶向药物也在市场上竞争。因此,索托拉西布需要通过良好的市场推广和价格策略来确保其在国内的成功。
总的来说,索托拉西布是一种颇具潜力的肺癌治疗药物,特别适用于那些携带有KRAS G12C突变的肺癌患者。虽然目前尚未在中国国内上市,但随着更多的研究数据的积累和药物监管机构的审批,我们可以期待索托拉西布在不久的将来为国内的肺癌患者带来新的治疗选择。

 全部分类
全部分类

 老挝第二制药
老挝第二制药
 美国安进
美国安进
 孟加拉珠峰制药
孟加拉珠峰制药
 老挝大熊制药
老挝大熊制药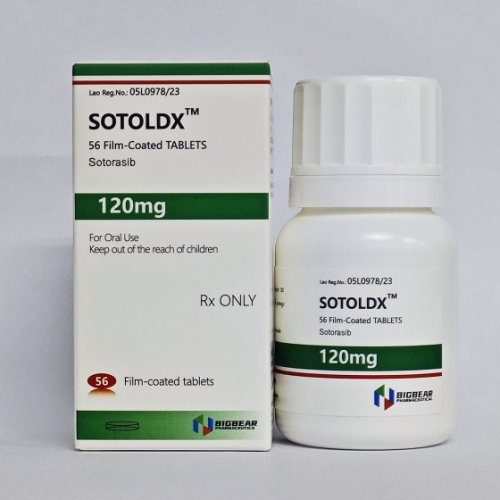

 中国贝达
中国贝达
 德国拜耳
德国拜耳
 日本第一三共
日本第一三共
 美国礼来Lilly
美国礼来Lilly



 粤ICP备2021070247号
粤ICP备2021070247号
